Làm thế nào để tìm số oxi hóa
NộI Dung
- giai đoạn
- Phần 1 Xác định số oxi hóa từ quy tắc hóa học
- Phần 2 Xác định số oxi hóa cho các nguyên tử không tuân theo quy tắc cụ thể
Trong hóa học, thuật ngữ "oxy hóa" và "khử" chỉ các phản ứng trong đó một nguyên tử (hoặc nhóm nguyên tử) lần lượt bị mất hoặc thu được electron. Số oxi hóa là số được gán cho các nguyên tử (hoặc nhóm nguyên tử) giúp các nhà hóa học biết có thể chuyển bao nhiêu electron và liệu thuốc thử có trải qua quá trình oxy hóa hay khử trong quá trình phản ứng. Quá trình mà một số nguyên tử hóa được gán cho các nguyên tử có thể đơn giản đến rất phức tạp tùy thuộc vào điện tích của các nguyên tử và thành phần hóa học của các phân tử mà chúng thuộc về. Để làm phức tạp thêm vấn đề, một số nguyên tử có thể có nhiều hơn hai số oxy hóa. May mắn thay, việc xác định số oxy hóa được điều chỉnh bởi các quy tắc được xác định rõ ràng, dễ thực hiện, mặc dù có thể có kiến thức về hóa học và đại số.
giai đoạn
Phần 1 Xác định số oxi hóa từ quy tắc hóa học
-

Xác định nếu sản phẩm bạn đang làm việc là một nguyên tử nguyên tố. Số oxi hóa của các nguyên tử cơ bản, tự do và không kết hợp với các nguyên tố khác, luôn là 0. Điều này đúng với các nguyên tử có dạng nguyên tố được tạo thành từ nguyên tử đơn giản này, nhưng cũng cho các nguyên tử có dạng nguyên tố là diatomic hoặc polyatomic.- Ví dụ: Al(S) và Cl2 cả hai đều có số oxi hóa bằng 0 vì chúng ở dạng nguyên tố, không có tổ chức.
- Lưu ý rằng dạng nguyên tố của lưu huỳnh, S8, hoặc octasulfur, mặc dù không đều, cũng có số oxi hóa là 0.
-

Xác định nếu sản phẩm được đề cập ở dạng ion hóa. Số oxi hóa của các ion bằng điện tích của chúng. Điều này đúng với các ion không liên kết với các nguyên tố khác mà còn đúng với các ion là một phần của hợp chất ion.- Ví dụ, số oxi hóa của ion Cl là -1.
- Cl ion sở hữu luôn luôn số oxi hóa -1 khi nó là một phần của hợp chất NaCl. Vì điện tích của ion Na, theo định nghĩa, là +1, nên chúng ta biết rằng điện tích của ion Cl là -1. Do đó, số oxi hóa của nó luôn là -1.
-

Đối với các ion kim loại, có thể có một số số oxy hóa. Nhiều yếu tố kim loại có nhiều hơn một tải. Ví dụ, sắt (Fe) có thể ở dạng ion hóa với điện tích +2 hoặc +3. Các điện tích của các ion kim loại (và do đó là số oxi hóa của chúng) có thể được xác định là hàm của các điện tích của các nguyên tử khác của hợp chất mà chúng là một phần, hoặc bằng cách khác sử dụng các số La Mã khi thông tin được viết dưới dạng e (như trong câu: "Điện tích của ion sắt (III) là +3").- Lấy ví dụ về hợp chất chứa ion kim loại nhôm. Hợp chất AlCl3 có tổng điện tích bằng 0. Chúng ta biết rằng các ion Cl có điện tích -1 và có 3 trong hợp chất, vì vậy ion Al phải có điện tích +3 để tổng điện tích của tất cả các ion bằng 0. Do đó, số oxi hóa của Al là +3.
-

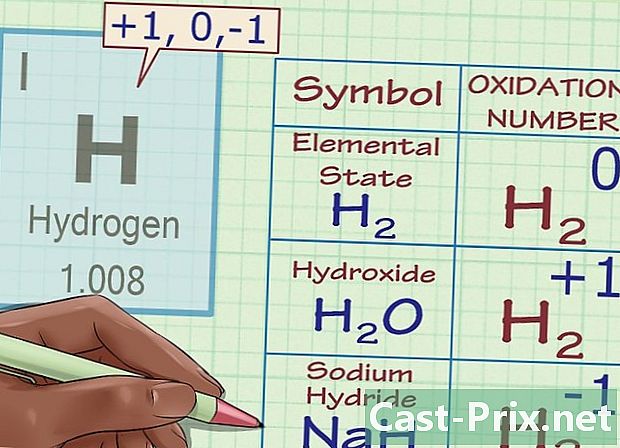
Chỉ định oxy một số oxy hóa -2 (với ngoại lệ). trong hầu hết Trong một số trường hợp, các nguyên tử oxy có số oxi hóa là -2. Tuy nhiên, có một số trường hợp ngoại lệ cho quy tắc này:- Khi oxy ở trạng thái nguyên tố (O2), số oxi hóa của nó là 0, như trường hợp của tất cả các nguyên tử cơ bản.
- Khi oxy là một phần của peroxide, sau đó số oxi hóa của nó là -1. Peroxit là một nhóm các hợp chất có liên kết oxy-oxy (hoặc peroxide anion) đơn giản2). Ví dụ, trong phân tử của H2O2 (hydro peroxide), số oxy hóa của oxy (và điện tích của nó) là -1.
- Khi oxy liên kết với flo, số oxi hóa của nó là +2. Để biết thêm thông tin, hãy đọc các quy tắc về florua sau trong bài viết này.
-

Chỉ định số oxi hóa +1 cho hydro (ngoại trừ). Đối với oxy, số lượng oxy hóa của hydro là trường hợp ngoại lệ. Nói chung, số oxy hóa của hydro là +1 (trừ khi, một lần nữa, nó ở dạng nguyên tố của nó, H2). Tuy nhiên, trong trường hợp đặc biệt được gọi là hợp chất lai, hydro có số oxi hóa là -1.- Ví dụ, trong phân tử của H2O, chúng ta biết rằng hydro có số oxi hóa +1 vì oxy có điện tích -2 và chúng ta cần điện tích 2 + 1 cho tổng điện tích của hợp chất là 0.Tuy nhiên, ở dạng lai của natri hydroxit, NaH, hydro có số oxi hóa -1 vì các ion Na có điện tích +1; do đó, để tổng điện tích của hợp chất bằng 0, điện tích hydro (và do đó số oxi hóa của nó) phải bằng -1.
-

Fluor có luôn luôn số oxi hóa -1. Như chúng ta đã đề cập, số lượng oxy hóa của các nguyên tố nhất định có thể thay đổi vì nhiều lý do (đây là trường hợp của các ion kim loại, nguyên tử oxy trong peroxit, v.v.). Tuy nhiên, flo có số oxi hóa là -1 và điều này không bao giờ thay đổi. Điều này là do thực tế là flo là nguyên tố có độ âm điện lớn nhất - nói cách khác, nó là nguyên tố có ít cơ hội nhất để cung cấp một trong số các điện tử của nó và có khả năng đảm nhận hoặc (các) electron của nguyên tố khác. Đó là lý do tại sao phí của anh ấy không thay đổi. -

Xét số oxi hóa của một hợp chất bằng với điện tích của hợp chất đó. Tổng các số oxi hóa của tất cả các nguyên tử của hợp chất phải bằng điện tích của hợp chất này. Ví dụ, nếu một hợp chất không được tích điện, tổng các số oxi hóa của tất cả các nguyên tử của nó phải bằng 0; nếu hợp chất là một ion điện tích đa nguyên -1, thì tổng các số oxi hóa phải là -1, v.v.- Đây là một cách tốt để kiểm tra xem bạn đã hoàn thành tốt công việc của mình chưa - nếu tổng số oxy hóa của hợp chất của bạn không bằng tổng điện tích của hợp chất, thì bạn có thể chắc chắn rằng mình đã nhầm lẫn. ở đâu đó trong việc xác định số oxy hóa của bạn.
Phần 2 Xác định số oxi hóa cho các nguyên tử không tuân theo quy tắc cụ thể
-

Tìm các nguyên tử không có quy tắc gán số oxi hóa. Đối với một số nguyên tử, không có quy tắc cụ thể để xác định số oxi hóa của chúng. Nếu nguyên tử của bạn không xuất hiện trong các đoạn trước và bạn không chắc chắn về điện tích của nó (ví dụ nếu nó là một phần của hợp chất lớn hơn và điện tích riêng lẻ không được cung cấp cho bạn), thì bạn có thể tìm số oxi hóa của nguyên tử bằng cách tiến hành khử. Đầu tiên, bạn sẽ xác định số oxi hóa của từng nguyên tử khác của hợp chất, trước khi xác định số nguyên tử mà bạn quan tâm dựa trên tổng điện tích của hợp chất.- Ví dụ, trong hợp chất Na2SO4, điện tích của lưu huỳnh (S) là không xác định - tất cả những gì chúng ta có thể nói là điện tích của nó khác 0 vì nó không ở dạng nguyên tố. Đó là một ứng cử viên tốt để áp dụng phương pháp đại số này để xác định số oxy hóa.
-

Tìm số oxi hóa của các nguyên tố khác của hợp chất. Sử dụng các quy tắc hóa học để xác định số oxi hóa, tìm số oxi hóa của các nguyên tử khác của hợp chất. Chú ý đến các trường hợp đặc biệt đối với các nguyên tử O, H, v.v.- Theo các quy tắc hóa học được nêu trong phần trước, chúng ta biết rằng trong hợp chất Na2SO4 các ion Na có điện tích (và do đó số oxi hóa) là +1 và các nguyên tử oxy có số oxi hóa là -2.
-

Đối với mỗi nguyên tử, nhân số của chúng với số oxi hóa của chúng. Bây giờ chúng ta đã biết số oxi hóa của tất cả các nguyên tử của chúng ta ngoại trừ nguyên tử quan tâm, chúng ta phải tính đến việc một số nguyên tử này có thể xuất hiện nhiều hơn một lần trong hợp chất. Nhân hệ số bằng số của mỗi nguyên tử (được viết bằng chỉ số sau ký hiệu hóa học của nguyên tử trong hợp chất) với số oxi hóa của nó.- Trong hợp chất Na2SO4chúng ta biết rằng có 2 nguyên tử Na và 4 nguyên tử O. Vì vậy, chúng ta phải nhân +1 (số oxi hóa Na) với 2 để thu được kết quả là 2, sau đó nhân -2 (số lượng oxy hóa O) bằng 4 để thu được kết quả là -8.
-
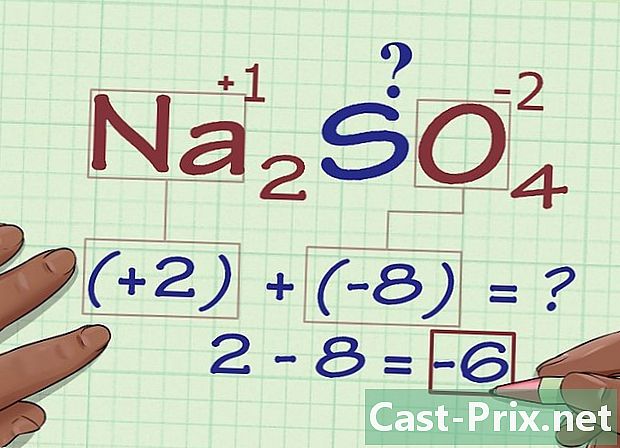
Thêm kết quả. Thêm kết quả của phép nhân của bạn để có được số oxi hóa mà không tính đến số oxi hóa của nguyên tử mà chúng ta quan tâm.- Trong ví dụ về Na2SO4, cần phải thêm 2 và -8 để nhận -6.
-
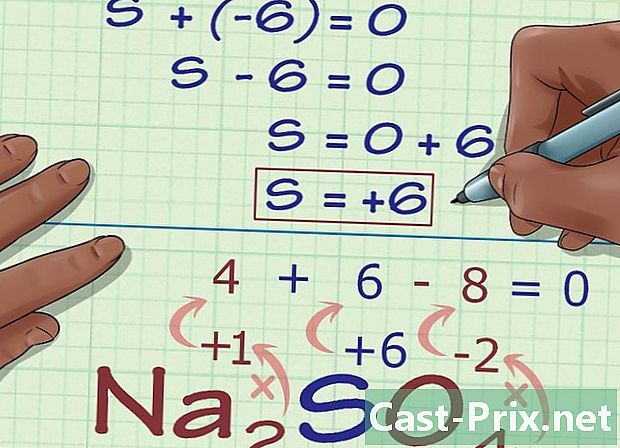
Tính số oxi hóa chưa biết dựa trên điện tích của hợp chất. Bây giờ bạn có tất cả các thông tin cần thiết để tìm số oxy hóa mà chúng ta quan tâm bằng cách sử dụng các quy tắc đại số đơn giản. Thiết lập một phương trình theo đó kết quả của các bước trước cộng với số oxi hóa chưa biết bằng với điện tích tổng thể của hợp chất. Nói cách khác: (Tổng các số oxi hóa đã biết) + (số oxi hóa chưa biết) = (điện tích hỗn hợp).- Bằng cách lấy ví dụ về Na2SO4Đây là cách thực hiện:
- (Tổng các số oxi hóa đã biết) + (số oxi hóa chưa biết) = (điện tích hỗn hợp)
- -6 + S = 0
- S = 0 + 6
- S = 6. Số oxi hóa của S bằng 6 trong hợp chất Na2SO4.
- Bằng cách lấy ví dụ về Na2SO4Đây là cách thực hiện:

